
News information
分类:行业资讯 发布时间:2023-04-18 访问量:1101
2023年美国癌症研究协会(AACR)年会正在火热举行,AACR是全球范围内备受瞩目的癌症研究会议之一。多家医药公司已经汇报各自疗法的最新临床试验结果,新锐公司也展现了创新抗癌治疗模式的广阔前景。今天这篇文章里,药明康德内容团队将与读者分享AACR大会上部分公布的最新临床期和临床前研究结果。

新抗原癌症疫苗迎来新时代?
Moderna和默沙东(MSD)公司宣布了个体化新抗原疫苗mRNA-4157与抗PD-1抗体Keytruda联用,治疗接受手术切除后高危恶性黑色素瘤(III/IV期)患者的2b期临床试验结果。中期结果显示,mRNA-4157与Keytruda联用,与Keytruda单药治疗相比,将患者复发或死亡风险降低了44%(HR=0.56,[95% CI,0.309-1.017];单侧p=0.0266)。接受组合疗法治疗的患者组中,22.4%的患者(n=24/107)出现复发或死亡,而单独接受Keytruda治疗的患者中,这一比例为40%(n=20/50)。联合治疗组的12个月无复发生存率为83.4%(95% CI,74.7-89.3),对照组为77.1%(95% CI,62.5-86.6)。

mRNA-4157是一款利用mRNA编码个体化新抗原的创新疗法,可以根据患者肿瘤DNA序列特征编码高达34种新抗原。当注入到患者体内后,这些mRNA产生的新抗原可以激活免疫系统,让患者产生针对肿瘤突变特征的个体化抗肿瘤免疫反应。这项研究代表着新抗原癌症疫苗领域的重大突破。“我对此感到非常兴奋。很高兴在这一领域耕耘了10多年后看到这样的数据。”丹娜-法伯癌症研究所的肿瘤学家Patrick Ott博士表示,“这是关键的一步。”
Moderna之外,BioNTech公司也在开发基于mRNA的新抗原癌症疫苗,其在研疗法BNT122治疗黑色素瘤患者的2期临床试验最新结果有望在今年公布。Gritstone bio公司的个体化癌症疫苗目前已经进入2/3期临床试验结果,一线治疗微卫星稳定结直肠癌患者。在2020年,Gritstone Oncology公司研究执行副总裁兼首席科学官Karin Jooss博士接受药明康德内容团队专访时曾表示,基于RNA技术的新疗法可以靶向更多新靶点,且具有成本优势,有望在五年内成为主要的治疗手段之一。
重磅免疫检查点抑制剂治疗肝癌、肺癌、胆管癌的最新结果
免疫检查点抑制剂已经在治疗转移性癌症患者方面获得卓越的效果,而将它们用于更早期癌症患者,降低癌症的复发和转移风险,达到潜在治愈,是抗癌疗法研究的重要方向之一。在AACR大会上,罗氏(Roche)公布了其PD-L1抑制剂Tecentriq与抗VEGF抗体Avastin联用,辅助治疗接受治愈性切除手术的高风险肝癌患者的3期临床试验结果。结果显示,在这一患者群体中,Tecentriq/Avastin组合将患者疾病复发风险降低28%。新闻稿指出,这是辅助治疗肝癌领域,首个获得积极结果的3期临床研究。
肝癌是世界上第六大常见癌症,几乎一半的病例在中国。早期患者可通过手术切除肿瘤,然而据统计,有高达80%的早期肝癌患者在手术后会产生复发。在这项研究中,中位随访时间为17.4个月时,Tecentriq/Avastin组合将患者癌症复发风险降低28%(HR=0.72,95% CI:0.56-0.93;P=0.0120)。总生存期数据尚未成熟。罗氏首席医学官兼全球产品开发负责人Levi Garraway博士表示:“Tecentriq/Avastin组合已经是治疗无法切除肝细胞癌的标准疗法,我们很高兴看到这些结果的潜力。”
此外,对病理学完全缓解(pCR)的最终分析显示,手术前使用Imfinzi加新辅助化疗的pCR率为17.2%,仅接受新辅助化疗的患者这一数值为4.3%。
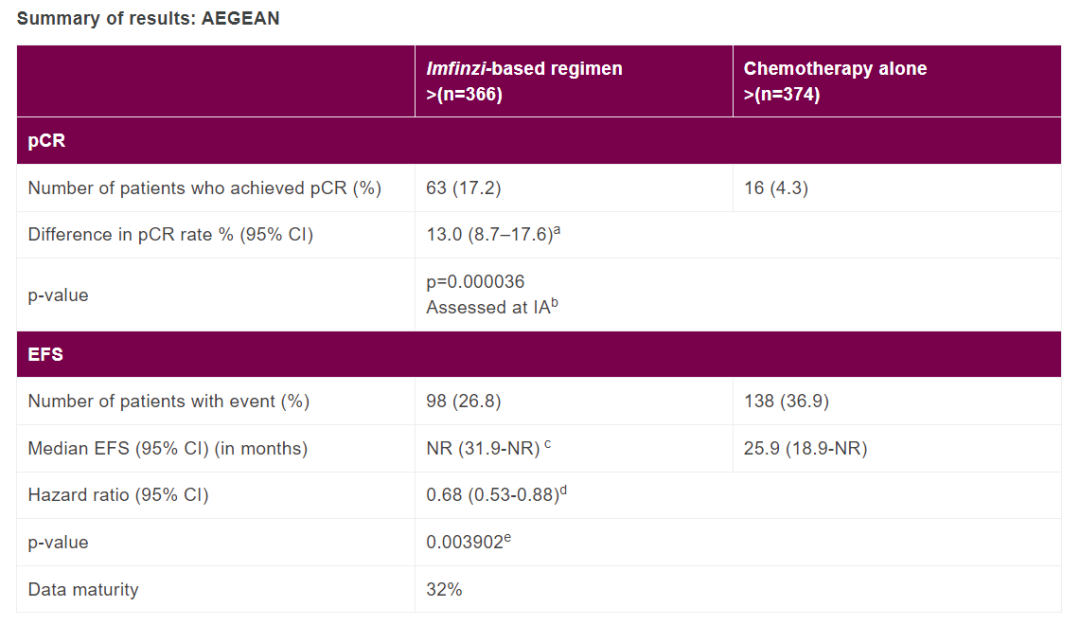
默沙东公司公布了Keytruda与化疗联用,一线治疗晚期或不可切除胆管癌患者的3期临床结果。结果显示,Keytruda与化疗联用,与化疗相比,显著提高这些患者的总生存期。在中位随访时间为25.6个月时,接受Keytruda联合化疗治疗的患者死亡风险比仅接受化疗的患者降低了17%(HR=0.83,95% CI,0.72-0.95;p=0.0034)。Keytruda组合的中位生存期为12.7个月(95% CI,11.5-13.6),而仅接受化疗的患者中位生存期为10.9个月(95% CI,9.9-11.6)。使用Keytruda/化疗组的一年生存率为52%,而仅接受化疗的一年生存率为44%;两年生存率分别为24.9%和18.1%。生存结果在亚组之间普遍一致。

靶向KRAS,礼来、信达生物公布最新结果
KRAS曾经是著名的不可成药靶点,近年来安进和Mirati Therapeutics公司靶向KRAS G12C突变体的抑制剂先后获得美国FDA的批准,代表着攻克KRAS不可成药性的重要突破。OMass Therapeutics首席执行官Ros Deegan女士在今年的药明康德全球论坛对攻克不可成药靶点表示乐观,她指出,不可成药靶点并非不可成药,而是尚未成药。目前业界拥有多种技术靶向这些靶点。

在AACR年会上,礼来公司(Eli Lilly)公布了其KRAS G12C抑制剂LY3537982的1期临床试验结果。在8位携带KRAS G12C突变,未接受过KRAS抑制剂治疗的经治NSCLC患者中,LY3537982达到38%的总缓解率和88%的疾病控制率。在14位曾接受过一种KRAS抑制剂治疗的患者中,总缓解率为7%,疾病控制率为64%。在20名结直肠癌患者中,LY3537982的总缓解率为10%,疾病控制率为90%。胰腺癌中的总缓解率和疾病控制率分别为42%和92%。

信达生物也公布了其KRAS G12C共价抑制剂IBI351(GFH925)的1期临床试验结果,在接受剂量为600 mg每日两次的IBI351治疗的NSCLC患者中,IBI351达到53.3%的确认客观缓解率和96.7%的疾病控制率。在这一群体中的中位无进展生存期(PFS)为8.2个月,9个月时的无进展生存率为47.3%。
新治疗模式展现抗癌潜力
AACR大会也是新锐公司展现前沿技术的舞台。今年的AACR大会上,由蛋白降解先驱,耶鲁大学教授Craig Crews教授联合创建的Halda Therapeutics公司公布了其调节诱导接近靶向嵌合体(RIPTAC)的临床前实验结果。RIPTAC的一端可以与肿瘤细胞中高度表达的蛋白相结合,而另一端与细胞内和细胞生存紧密相关的蛋白结合。它们构成的三元复合体会抑制维持细胞生存蛋白的功能,从而导致肿瘤细胞的死亡。而健康细胞因为蛋白表达水平不高,不会被RIPTAC分子杀死。
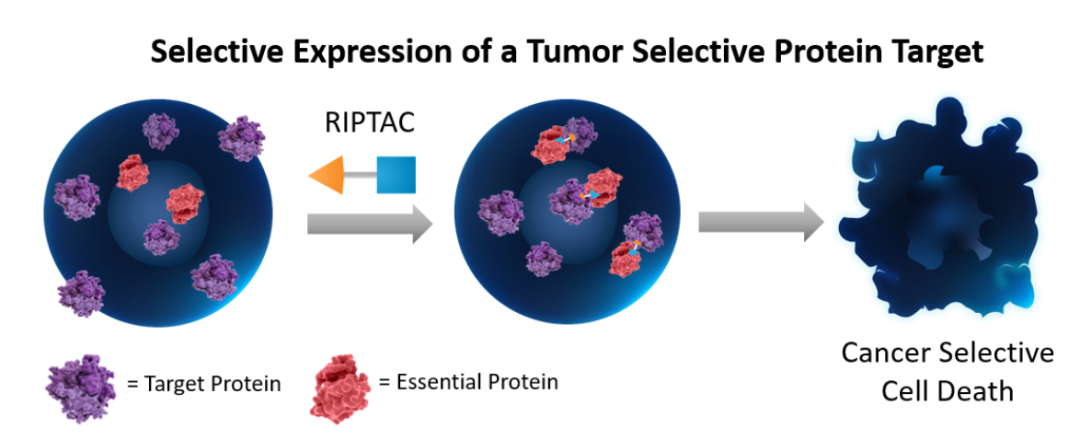
图3 ▲RIPTAC分子的作用机制
在AACR大会上公布的数据显示,靶向雄激素受体(AR)的多种在研RIPTAC分子在对恩杂鲁胺耐药的前列腺癌小鼠模型中,与恩杂鲁胺相比,显示出更好的口服抗癌活性。
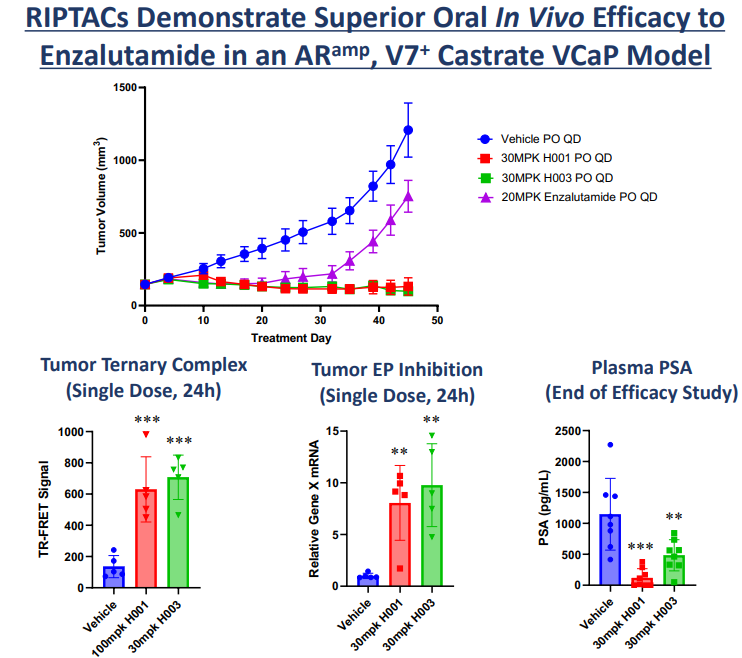
图4 ▲RIPTAC分子的体内临床前研究数据
Affimed公司公布了其先天细胞衔接蛋白(innate cell engager,ICE)AFM13治疗复发/难治性外周 T 细胞淋巴瘤(PTCL)的2期临床试验结果。AFM13是一种4价双特异性蛋白,可以将自然杀伤(NK)细胞募集到CD30阳性PTCL周围,并且增强NK细胞介导的抗体依赖性细胞毒性。

试验结果显示,AFM13表现出强大的活性,达到试验主要终点,意向治疗(ITT)人群的客观缓解率(ORR)为32.4%,完全缓解率(CR)为10.2%。患有血管免疫母细胞淋巴瘤(AITL)的患者表现出最高的ORR(53.3%)和CR(26.7%)。这是PTCL最常见的亚型之一。
期待这些获得积极进展的疗法进展顺利,早日造福更多癌症患者。
来源于网站,如有侵权请联系删除。

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。
2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。